Les LASA sous haute surveillance
 Plus les étapes liées à la préparation d’un médicament sont nombreuses, plus les risques augmentent. C’est le cas des injectables qui ont un éventail d’applications étendu. Ils sont employés en anesthésie, réanimation, chimiothérapie, nutrition, ou encore en antibiothérapie. Compte tenu de la voie d’administration utilisée, ils requièrent prudence et vigilance jusqu’à l’administration et exigent une surveillance accrue lorsque la prescription implique des médicaments appelés Look-Alike et/ou Sound-Alike, les LASA.
Plus les étapes liées à la préparation d’un médicament sont nombreuses, plus les risques augmentent. C’est le cas des injectables qui ont un éventail d’applications étendu. Ils sont employés en anesthésie, réanimation, chimiothérapie, nutrition, ou encore en antibiothérapie. Compte tenu de la voie d’administration utilisée, ils requièrent prudence et vigilance jusqu’à l’administration et exigent une surveillance accrue lorsque la prescription implique des médicaments appelés Look-Alike et/ou Sound-Alike, les LASA.
À la fin des années 60, seule une dizaine de produits était concernée par leur ressemblance, qu’elle soit visuelle (Look-Alike) ou phonétique (Sound-Alike). Elle se retrouve dans le nom, la forme ou le conditionnement. On estime aujourd’hui à plus de 3 000 le nombre de paires, parfois de trios, de LASA. Principale responsable ? La chute des brevets. Elle a provoqué l’arrivée de très nombreux médicaments génériques avec des noms similaires pour un même principe actif. C’est notamment le cas des anti-infectieux. Les confusions génèrent de nombreux accidents aux conséquences potentiellement fatales car elles impliquent parfois des substances dangereuses telles que de puissants tranquillisants ou des anticancéreux.
 Les LASA représentent à eux seuls un quart des erreurs médicamenteuses signalées aux États-Unis. Pour réduire leur impact sur la sécurité des patients, de multiples mesures ont été engagées. Tout d’abord, au niveau de la prescription, première étape critique dès la lecture lorsqu’elle est manuscrite, elle s’est peu à peu informatisée. Elle contient avec exactitude les informations importantes sur le médicament et sa préparation. Concentration, dosage, diluant, vitesse de perfusion, autant de précisions indispensables pour éviter les confusions, sécuriser la reconstitution au sein de la pharmacie hospitalière ainsi que l’administration au patient. Toujours dans le milieu hospitalier, de nombreuses recommandations ont été rédigées. Elles préconisent entre autres de ne pas acheter plusieurs médicaments génériques pour un même principe actif, mais aussi une meilleure organisation du stockage des injectables en séparant les produits dangereux des autres ou un étiquetage additionnel pour mieux les identifier.
Les LASA représentent à eux seuls un quart des erreurs médicamenteuses signalées aux États-Unis. Pour réduire leur impact sur la sécurité des patients, de multiples mesures ont été engagées. Tout d’abord, au niveau de la prescription, première étape critique dès la lecture lorsqu’elle est manuscrite, elle s’est peu à peu informatisée. Elle contient avec exactitude les informations importantes sur le médicament et sa préparation. Concentration, dosage, diluant, vitesse de perfusion, autant de précisions indispensables pour éviter les confusions, sécuriser la reconstitution au sein de la pharmacie hospitalière ainsi que l’administration au patient. Toujours dans le milieu hospitalier, de nombreuses recommandations ont été rédigées. Elles préconisent entre autres de ne pas acheter plusieurs médicaments génériques pour un même principe actif, mais aussi une meilleure organisation du stockage des injectables en séparant les produits dangereux des autres ou un étiquetage additionnel pour mieux les identifier.
Autre action préventive concrète, la typographie du médicament sur son emballage primaire et secondaire. La casse des lettres, minuscule et majuscule, a été alternée pour mieux identifier les syllabes différentes. L’utilisation des lettres majuscules a nettement amélioré la lisibilité du nom du produit. Plus récemment aux États-Unis, l’Institut pour des Pratiques Médicales Sécurisées, (ISMP ou Institute for Safe Medication Practices) est allé plus loin. Il recommande désormais d’accentuer la visibilité en incorporant des caractères gras : LOOK-Alike & SOUND-Alike.
Réglementaires et packaging, des solutions existent
De nombreux organismes gouvernementaux tels que l’ANSM ou la FDA ont publié une liste qui regroupe l’ensemble des médicaments LASA. Elle est régulièrement mise à jour, mais il est difficile, voire impossible, de l’harmoniser sur un plan international. Beaucoup de produits pharmaceutiques ont en effet un nom différent selon le pays où ils sont commercialisés. Toujours d’un point de vue réglementaire, il est possible d’agir en amont, notamment avant d’accorder une mise sur le marché. Lors du dépôt du dossier, un nom commercial qui ne soit pas similaire à un produit déjà existant pourrait être exigé sous peine de refus d’approbation.
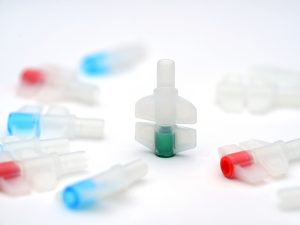 Côté packaging, une autre solution est envisageable et facilement réalisable : l’attribution d’un code couleur par catégorie de produits qui serait visible sur les emballages primaires et secondaires. Dans le cas des médicaments injectables conditionnés en poches souples, les ports d’administration tels que les twist-off ou les luer-lock pourraient afficher des couleurs spécifiques (bleu, rouge, vert, etc.) selon les produits. Pour les autres formulations, la couleur serait apparente sur l’emballage secondaire et l’étiquetage du produit.
Côté packaging, une autre solution est envisageable et facilement réalisable : l’attribution d’un code couleur par catégorie de produits qui serait visible sur les emballages primaires et secondaires. Dans le cas des médicaments injectables conditionnés en poches souples, les ports d’administration tels que les twist-off ou les luer-lock pourraient afficher des couleurs spécifiques (bleu, rouge, vert, etc.) selon les produits. Pour les autres formulations, la couleur serait apparente sur l’emballage secondaire et l’étiquetage du produit.
De nombreuses pistes d’améliorations sont donc envisageables pour réduire les risques d’erreurs liés aux médicaments Look-Alike et Sound-Alike. Mais pour les mettre en application, seule une collaboration internationale entre l’industrie pharmaceutique, les industriels du packaging, les organismes réglementaires et les utilisateurs finaux permettrait de lever les dernières barrières.
Sylvie Ponlot


















